蛋白质分子的空间结构
蛋白质分子并非如一级结构那样是完全展开的“线状”,而是处于更高级的水平。天然蛋白质可折叠、盘曲成—定的空间结构(三维结构)。蛋白质的空间结构指蛋白质分子内各原子围绕某些共价键的旋转而形成的各种空间排布及相互关系,这种空间结构称为构象。按不同层次,蛋白质的高级结构可分为二,三和四级结构。
蛋白质的二级结构
多肽链主链中各原子在各局部的空间排布,即多肽链主链构象称为蛋白质的二级结构。
(1)形成二级结构的基础——肽键平面:20世纪30年代末,Pauling L和Corey R开始对肽进行x射线结晶衍射图研究,以探索蛋白质的精细结构。他们测定了分子中各原子间的标准键长和键角,发现肽单元(主链的-CαCN-)呈刚性平面(rigid plane),即肽键平面。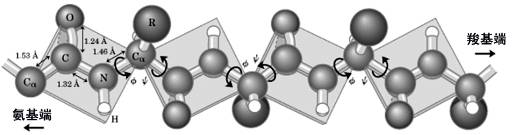
(2)蛋白质二级结构的基本形式:蛋白质的肽链局部盘曲、折叠的主要有α-螺旋、β-折叠、β-转角和不规则卷曲等几种形式。
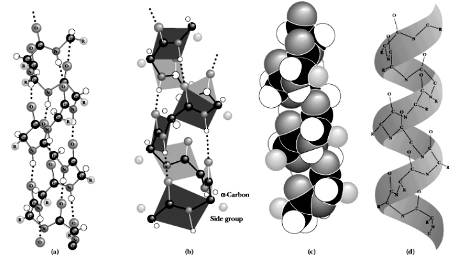
1) α-螺旋:肽链的某段局部盘曲成螺旋形结构,称为α-螺旋(图12)。 α-螺旋的特征是:①—般为右手螺旋;②每螺旋圈包含3.6个氨基酸残基,每个残基跨距为0.15nm,螺旋上升1圈的距离(螺距)为3.6×0.15=0.54nm; = 3 \* GB3 ③螺旋圈之间通过肽键上的>C=O和-NH-间形成氢键以保持螺旋结构的稳定;④影响α-螺旋形成的主要因素是氨基酸侧链的大小、形状及所带电荷等性质。
蛋白质分子并非如一级结构那样是完全展开的“线状”,而是处于更高级的水平。天然蛋白质可折叠、盘曲成—定的空间结构(三维结构)。蛋白质的空间结构指蛋白质分子内各原子围绕某些共价键的旋转而形成的各种空间排布及相互关系,这种空间结构称为构象。按不同层次,蛋白质的高级结构可分为二,三和四级结构。
蛋白质的二级结构
多肽链主链中各原子在各局部的空间排布,即多肽链主链构象称为蛋白质的二级结构。
(1)形成二级结构的基础——肽键平面:20世纪30年代末,Pauling L和Corey R开始对肽进行x射线结晶衍射图研究,以探索蛋白质的精细结构。他们测定了分子中各原子间的标准键长和键角,发现肽单元(主链的-CαCN-)呈刚性平面(rigid plane),即肽键平面。

肽键平面和Cα“关节”示意图
由于C-N键具有部分双键性质,因此C=O和C—N均不能自由旋转。所以整个肽链的主链原子(-CαCN-CαCN-)中只有N-Cα和Cα-N之间的单键可以旋转,N -Cα之间的旋转角为φ (phi),Cα-C之间的旋转角为ψ(psi)。φ和ψ的大小就决定了Cα相邻两个肽键平面之间的相对位置关系,于是肽键平面就成为主链构象的结构基础。如每个氨基酸的ψ和φ已知,整个多肽链的主链构象就确定了。(2)蛋白质二级结构的基本形式:蛋白质的肽链局部盘曲、折叠的主要有α-螺旋、β-折叠、β-转角和不规则卷曲等几种形式。
1) α-螺旋:肽链的某段局部盘曲成螺旋形结构,称为α-螺旋(图12)。 α-螺旋的特征是:①—般为右手螺旋;②每螺旋圈包含3.6个氨基酸残基,每个残基跨距为0.15nm,螺旋上升1圈的距离(螺距)为3.6×0.15=0.54nm; = 3 \* GB3 ③螺旋圈之间通过肽键上的>C=O和-NH-间形成氢键以保持螺旋结构的稳定;④影响α-螺旋形成的主要因素是氨基酸侧链的大小、形状及所带电荷等性质。

α-螺旋示意图
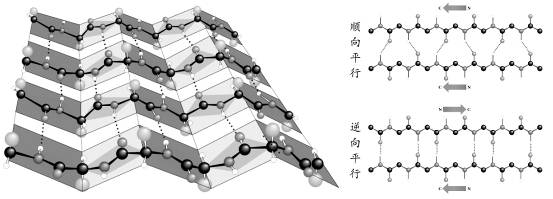
2)β-折叠:为―种比较伸展、呈锯齿状的肽链结构。两段以上的β-折叠结构平行排布并以氢键相连所形成的结构称为β-片层或β-折叠层。β-片层可分顺向平行(肽链的走向相同,即N、C端的方向一致)和逆向平行(两肽段走向相反)结构。

β—折叠结构示意图
3) β-转角:此种结构指多肽链中出现的一种180°的转折。β-转角通常由4个氨基酸残基构成,由第1个残基的>C=O与第4个残基的-NH-形成氢键,以维持转折结构的稳定。
4)不规则卷曲:此种结构为多肽链中除以上几种比较规则的构象外,多肽链中其余规则性不强的—些区段的构象。

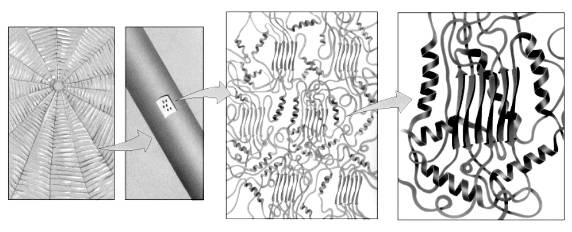
蜘蛛网丝蛋白