多肽链中,各个二级结构的空间排布方式及有关侧链基团之间的相互作用关系,称为蛋白质的三级结构。换言之,蛋白质的三级结构系指每一条多肽链内所有原子的空间排布,即多肽链的三级结构=主链构象+侧链构象,三级结构是在二级结构的基础上由侧链相互作用形成的。
多肽链的侧链(也就是氨基酸的侧链)分为亲水性的极性侧链和疏水性的非极性侧链(详见氨基酸分类)。水介质中球状蛋白质的折叠总是倾向于把多肽链的疏水性侧链或疏水性基团埋藏在分子的内部。这一现象被称之为疏水作用或疏水效应。疏水作用的本质是疏水基团或疏水侧链出自避开水的需要而被迫相互靠近,并不是疏水基团之间有什么吸引力的缘故,因此,将疏水作用称之为“疏水键”是不正确的。疏水作用是维系蛋白质三级结构最主要的动力。除疏水作用外,维系蛋白质的三级结构的动力还有氢键、盐键(离子键)、范德华力和二硫键等。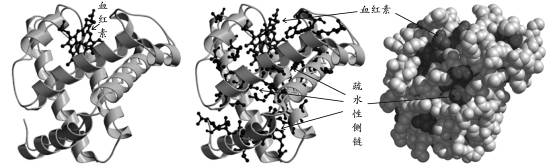
多肽链的侧链(也就是氨基酸的侧链)分为亲水性的极性侧链和疏水性的非极性侧链(详见氨基酸分类)。水介质中球状蛋白质的折叠总是倾向于把多肽链的疏水性侧链或疏水性基团埋藏在分子的内部。这一现象被称之为疏水作用或疏水效应。疏水作用的本质是疏水基团或疏水侧链出自避开水的需要而被迫相互靠近,并不是疏水基团之间有什么吸引力的缘故,因此,将疏水作用称之为“疏水键”是不正确的。疏水作用是维系蛋白质三级结构最主要的动力。除疏水作用外,维系蛋白质的三级结构的动力还有氢键、盐键(离子键)、范德华力和二硫键等。

肌红蛋白三级结构
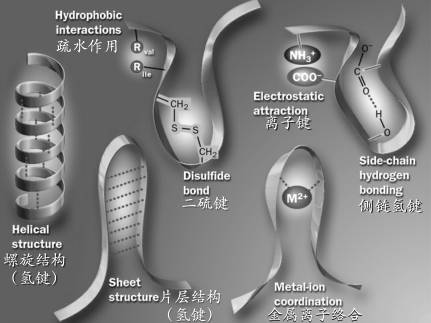
蛋白质中的肽键称为主键,氢键、盐键、疏水作用、离子键、二硫键等是副键(次级键,图16),副键因外力作用(如热)容易断裂,导致蛋白质变性失活。
稳定和维系蛋白质三级结构的键
三级结构对于蛋白质的分子形状及其功能活性部位的形成起重要作用,通过三级结构的形成,可将肽链中某些局部的几个二级结构汇成“口袋”或“洞穴”状,这种结构称为结构域(domain),它们的核心部分多为疏水氨基酸构成,结合蛋白质的辅基常镶嵌在其中,这种结构域多半是蛋白质的活性部位。有的蛋白质分子中只有一个特异的结构域,有的则有多个结构域。最近,在很多蛋白质分子中发现有两段β-折叠之间通过一段α-螺旋相连而形成的球状结构,以及多个α-螺旋形成的螺旋束,或三个二硫键将肽链连接成的三环状结构等结构域与功能活性有密切关系。